Гальваническое железнение в домашних условиях
Гальваника дома. Советы и рецепты
Гальваникой часто занимаются мастера хендмейда, делающие  сувениры для души или на продажу. Распространено омеднение неметаллических предметов: керамических поделок, ракушек, птичьих перышек, листиков, веточек с деревьев, цветов, желудей и т.п.
сувениры для души или на продажу. Распространено омеднение неметаллических предметов: керамических поделок, ракушек, птичьих перышек, листиков, веточек с деревьев, цветов, желудей и т.п.
Советы
Для того, чтобы загальванизировать неметаллический предмет, его следует покрыть токопроводящим слоем. Для бытовых условий лучше всего подходит графитовый лак в форме спрея. Для создания графитового слоя достаточно обрызгать предмет со всех сторон, высушить в течение 15-30 минут и несколько раз повторить процедуру.
Для создания двустороннего равномерного покрытия нужно использовать два анода, разместив предмет для гальванизации между анодами. Толщина покрытия зависит от времени, в течение которого предмет будет находиться в электролите. Чем дольше длится гальванирование, тем толще получится слой металла на поверхности.
Перед гальванированием металлической детали ее нужно тщательно очистить от пыли, мелких заусенцев, тщательно обезжирить и высушить.
После того, как предмет загальванизирован, его нужно промыть в чистой воде, после чего можно брать в руки.
 |
 |
 |
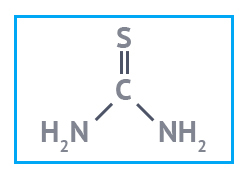
| Желатин пищевой 180 блюм 8 | Тиомочевина «ч» | Медь сернокислая 5-водная «ч» |
Рецепты электролитов
Для омеднения чаще всего применяют серный электролит, состоящий из медного купороса и серной кислоты. Серная кислота улучшает электропроводимость раствора. Дополнительно вводятся различные добавки, которые стабилизируют электролит, делают покрытие более блестящим (если нужно). Ввод блескообразователей позволяет получить зеркальную глянцевую поверхность без последующей механической обработки готового покрытия. Но одновременно, делает покрытие хрупким, не эластичным.
Все используемые реактивы должны быть максимальной химической чистоты, т. к. примеси могут ухудшить процесс гальванирования и качество получаемого покрытия.
- Для матового эластичного покрытия на 1 л раствора потребуется:
- 200 г сухого порошка медного купороса (желательно очищенного, категории ч или хч)
- 160 г серной кислоты
- 1,5 мл этанола (можно отмерить шприцом) или фенола
- 2-4 крупинки гранулированного желатина
Для приготовления электролита сначала нагревается пол литра дистиллированной воды до температуры около +80 °С, в воде растворяется медный купорос, раствор процеживается. В него добавляется серная кислота, потом объем раствора доводится до 1 л. Добавляются все остальные ингредиенты, затем раствор на несколько часов ставится остывать и отстаиваться.
Омеднение по данному рецепту будет матовым, но зато перышко или листик с дерева можно гнуть или придать ему нужную форму, нагрев изделие. Если хочется, то изделию можно придать глянцевый блеск тщательной шлифовкой, но иногда это сделать сложно, нужны специальные приспособления, например, гравер.
- Рецепт для получения блестящего медного покрытия. На 1 л раствора надо:
- 200 г медного купороса
- 130 г серной кислоты
- 1 капля унитиола (продается в аптеках)
- примерно 0,07 г тиомочевины
- 0,05 г поваренной соли
Покрытие получится блестящим, но не подходит для гнущихся предметов. Этот вид электролита можно использовать для получения полированного финишного покрытия не только для сувениров, но и для технических деталей.
Гальваническое травление. Безопасный способ
С помощью гальванического процесса можно не только покрывать поверхность детали тонкой металлической пленкой, но и вытравливать рисунки на металлической поверхности (лезвие ножа, столовый прибор, что-либо другое). Гальваническое травление позволяет получить рисунки с четкими очертаниями, гладкими краями и глубиной одинаковой величины. Для этого потребуется тоже самое оборудование, что и для гальванирования, но в данном процессе анодом будет выступать протравливаемая деталь. Обычно таким способом вытравливают поверхности из нержавеющей, устойчивой к кислотам стали, которую сложно или даже невозможно травить химическим способом.
Процесс травления: 
- деталь тщательно отполировать, промыть, обезжирить (например, спиртом), слегка нагреть, нанести на нее слой воска; по воску выполнить желаемый рисунок, процарапывая воск до металла;
- предмет и медную пластину укрепить на штангах в гальванической ванне так, чтобы рисунок был обращен к медной пластине; расстояние между деталью и пластиной — около двух сантиметров;
- залить в емкость насыщенный раствор поваренной соли (4 столовые ложки на 1 л дистиллированной воды), подключить источник тока (например, зарядное устройство от мобильного телефона), плюсовый контакт на деталь, минусовый — на медную пластину;
- подождать примерно 40 минут;
- вынуть деталь, промыть в воде, нагреть и удалить воск.
Вместо воска можно использовать лак для ногтей, битумный лак или специальную грунтовку. Вместо соли — химически чистый медный купорос. Вместо медной пластины можно взять предмет из стали или железа, например, саморез, гвоздь.
Эта технология подходит не только для стальных поверхностей, но и для предметов из цинка, никеля, меди, латуни. Но для них требуются другие химикаты, гораздо более вредные, поэтому в домашних условиях их не используют.
Гальваническое железнение. Есть результат!
Есть изношенная деталь и ну очень нужно ее восстановить. Деталь железная. Нагрузка на стороне, которую буду восстанавливать — только ударная, трения нет. Нужно нарастить слой примерно 0,07 мм.
Собственно поискал в интернете. Хочу уточнить по элеткролитам: можно ли использовать раствор FeCl3 (тот, что используется для травления плат в радиотехнике), а если нельзя, то какой можно использовать электролит из доступных в свободной продаже?
- Вход или Регистрация
Да, так же еще интересует, каких образом можно защитить те части детали, которые не нужно наращивать? Можно ли покрыть воском, нитролаком?
- Вход или Регистрация
мне чет кажется , что хлорид железа лучше не использовать , по крайней мере при восстановлении чугуния и люминя , я ни разу не встречал FeCl3 ни в простых ни в сложных многокомпонентных электролитах .
- Вход или Регистрация
Ok , ток не сёдня , потомучто сёдня я стал настоящим дядя pSicHo с большой буквы ( седня племянница неожиданно с утра родилась ) , так что теперь не знаю даже ка к ник переделать лаконичней 🙂
- Вход или Регистрация
Нашел вот такой рецепт:
Электролит для железнения (твердое покрытие)
Сернокислый железоаммоний . 350 г
Серная кислота концентрированная . 0,25 г
Вода . до 1 л
Электролит используется при температуре 18-20°С, плотность тока 2 А/дм2
Что есть «Сернокислый железоаммоний» и где его можно приобрести?
- Вход или Регистрация
Думается мне, имелись в виду железоаммонийные квасцы Fe(NH4)(SO4)2
Где найти — в Яндексе посмотри, кто из производителей-продавцов поближе.
- Вход или Регистрация
моно просто сеенокислое железо FeSO4 пирменить , там кстати помоему все рецепты делаются на литр воды
- Вход или Регистрация
Ну в основном везде советуется применять раствор FeCl2 c небольшим добавлением соляной кислоты.
- Вход или Регистрация
Для восстановления рабочих поверхностей гнезд корпусов А. Н. Заикиной разработаны и проверены на гнездах коренных подшипников алюминиевых блоков двигателей Заволжского моторного завода (ЗМЗ) специальные электролит и анод , которые с успехом можно использовать. Конструкция анода (а. с. № 685727) показана на рис. 5.8. Как видно из рисунка, анод выполнен полым, облицован поролоном, имеет по наружной поверхности три косых среза. При работе чаша анода заполняется электролитом; свободный проход электролита и обильное смачивание адсорбирующего материала (поролона) обеспечиваются за счет трех рядов отверстий в каждом секторе электрода. Плоские срезы на наружной поверхности обеспечивают прерывистость электролитического процесса при вращении анода. Хорошее и равномерное смачивание поролона по всей его высоте и окружности и уменьшение угла контакта электродов за счет срезов способствуют равномерному распределению силовых линий электрического поля и образованию равномерного по толщине слоя покрытия поверхности отверстия восстанавливаемой детали. Электролит (а. с. № 755897) отличается некоторой сложностью (многокомпонентностью). Объясняется это тем, что блоки двигателей ЗМЗ, выполнены из алюминиевого сплава, а крышки коренных подшипников из ковкого чугуна. Состав электролита следующий (г/л):
Сернокислый цинк (ZnSO4) 225 ± 25
Сернокислый никель — аммоний [NiSO4·(NH4)2SO4] 35 ± 5
Сернокислый алюминий [Al2(SO4)3] 25 ± 5
Сернокислое закисное железо (FeSO4) 15 ± 5
Сернокислый натрий (Na2SO4) 1-3
Аскорбиновая кислота (Витамин С) 1-4
Фтористый натрий (NaF) 20 ± 5
Роль перечисленных компонентов в основном такая: фтористый натрий способствует разрушению окисных пленок и растравливанию алюминиевых поверхностей при анодной обработке; сернокислое железо (закисное), сернокислый натрий и аскорбиновая кислота обеспечивают хорошую адгезию с алюминиевой поверхностью и достаточную микротвердость и износостойкость нарощенного металла. Кроме того, сернокислый натрий способствует образованию мелкокристаллической структуры; сернокислый алюминий обеспечивает необходимую кислотность раствора; сернокислый цинк и сернокислый никель-аммоний введены в состав электролита потому, что цинк и никель характеризуются хорошей сцепляемостью со стальной или чугунной основой. Применительно к гнездам подшипников, выполненных только из алюминиевого сплава, содержание последних двух компонентов, вероятно, можно скорректировать. Рекомендуемый режим восстановления поверхностей в электролите приведенного состава: постепенное увеличение плотности тока с 7 до 70 А/дм2 в течение 10-15 мин с выдержкой на максимуме 5 мин; температура 20-25 °С; кислотность РН = 2-3; анодное травление в электролите в течение 1-2 мин.

Звягин А.А. и др. «Автомобили ВАЗ, изнашивание и ремонт» Л., Политехника, 1991, стр. 230-233
- Вход или Регистрация
Износ устраняют натиранием.
С.Я. Ландо
Изношенные отверстия в корпусных деталях чаще всего ремонтируют методом постановки втулки. Процесс этот довольно трудоемкий, поэтому нередко такие детали заменяют новыми. Иногда для восстановления изношенных отверстий в деталях из чугуна и алюминиевых сплавов целесообразно применять электронатирание. Электронатирание — один из методов нанесения гальванических покрытий. Этот процесс относится к вневанным способам наращивания на поверхность гальванических покрытий. Сущность его заключается в том, что к детали (катоду) подключают провод, идущий от отрицательного полюса источника питания постоянным током. Анодом служит угольный или металлический стержень, который обертывают специальным адсорбирующим материалом, пропитывают электролитом и соединяют с положительным полюсом. Переход металла с электролита на восстанавливаемую деталь осуществляется во время перемещения анода по покрываемой поверхности. Материал, на который постоянно поступает электролит, служит как бы электролитической ванной, и при включенном токе начинается процесс электролиза. Положительно заряженные ионы металла, находящиеся в электролите, соприкасаясь с поверхностью отрицательно заряженной детали, восстанавливаются и отлагаются в виде атомов металла. Электронатиранием можно ремонтировать изношенные отверстия под подшипники в тех местах, где во время работы деталь не испытывает большие силовые нагрузки, например, в корпусах водяных насосов, крышках генераторов, картерах коробок передач и т. п. При восстановлении отверстий в таких деталях, как вращатель анодного приспособления, может быть использован вертикальносверлильный или какой другой станок, у которого шпиндель крутится со скоростью 22–28 об/мин, а в качестве источника тока применен любой выпрямитель или генератор постоянного тока напряжением не ниже 30 В. Анод изготавливают из стального круга. Его диаметр после обработки должен быть на 3–4 мм меньше диаметра восстанавливаемого отверстия. Конусная часть остова анода должна входить в шпиндель станка и прочно в нем удерживаться. На цилиндрическую часть остова анода плотно наматывают какуюнибудь ткань, хорошо впитывающую жидкость, например сукно. Диаметр анода с навернутым на него материалом должен быть таким же, как диаметр восстанавливаемого отверстия, т. е. при вращении анода в отверстии детали материал должен прилегать к его стенкам. Для перекачки электролита из поддона к месту электронатирания применяют насос. Технологический процесс восстановления изношенных отверстий гальваническим электронатиранием состоит из следующих операций: мойки деталей и зачистки поверхности отверстий шлифовальной лентой, обезжиривания отверстий 50%-ным раствором едкого натра, травления поверхности отверстия 20%-ным раствором соляной кислоты, декапирования, гальванического натирания,. обезжиривания ацетоном и промывки в горячей и холодной воде.
После соответствующей подготовки детали и отверстия ее закрепляют на стол станка, предварительно отцентрировав относительно шпинделя отверстие, опускают в него анод, включают насос подачи электролита, станок и источник тока. В начале процесса к детали подключают плюсовой провод от источника тока, при этом происходит декапирование поверхности отверстия. Через 30–50 сек переключают полярность источника тока на обратную, при которой положительный полюс подсоединен к вращающемуся аноду. С этого момента начинается осаждение на деталь металла. По окончании натирания выпрямитель и насос подачи электролита выключают, извлекают анод из отверстия детали и снимают ее со станка. Затем калибром проверяют диаметр восстановленного отверстия. Для натирания чугунных деталей применяют электролит следующего состава: сернокислый цинк 600 г/л, борная кислота 30 г/л. Для натирания деталей из алюминиевых сплавов электролит составляют из сернокислого цинка (600 г/л) и сернокислого алюминия (30 г/л). Вот режимы электронатирания деталей: температура электролита (°С) 18–23, кислотность электролита (рН) 3,5–4,5, плотность тока (А/дм2) 180–220, напряжение (В) 25–28. При этом режиме на поверхности отверстия отлагается слой металла толщиной: за 1–2 мин. 0,1–0,15 мм, за 2–3 мин. 0,15–0,20 мм, за 3–4 мин. до 0,3 мм. После восстановления отверстия гальваническим натиранием не требуется никаких дополнительных механических операций для обработки лишнего слоя, так как при запрессовке подшипника лишний металл снимается его обоймой. В заключение для сравнения добавим, чтобы восстановить деталь с изношенным отверстием методом постановки втулки, надо затратить в 6–8 раз больше времени, чем способом электронатирания.
С.Я. Ландо «Это Вы можете.» Московский рабочий 1987, стр. 82
Меднение в домашних условиях
Содержание статьи: 
Меднение в домашних условиях – это технологический процесс, позволяющий наносить на металл, а также другие материалы (вольфрам, сталь) слой меди толщиной от 1 до 300 мкм. Покрытие медным слоем обеспечивает хорошую адгезию металла и при увеличении толщины покрытий придает блеск изделиям, устраняет небольшие дефекты, позволяет создавать копии вещи. Удивительно, но все это можно делать и самим. Сегодня мы расскажем, как осуществить меднение металла в домашних условиях.
Гальваника медью в домашних условиях: общие сведения

С технической точки зрения обработка – это электрохимический процесс. В процессе всегда есть два «участника» анод+электролит (источник металла) и деталь.
Технология гальваники медью в домашних условиях достаточно проста. Заключается она в том, что за счет электролита и проводимого через него тока выделяются атомы металла. Они оседают на поверхности, образуя медное покрытие.
Среди основных этапов гальванического меднения в домашних условиях:
- Подготовка поверхности (механическая и химическая).
- Нанесение подслойного покрытия (если необходимо)
- Меднение в соответствующем исходному металлу электролите.
Для декоративного гальванического меднения подойдут электролиты матового и блестящего меднения. После нанесения слоя, можно обработать поверхность в электролитах серебра, золота никеля и т.д.
Необходимые инструменты для меднения в домашних условиях

«Ингредиенты», без которых меднение не состоится, но которые реально подготовить в домашних условиях. Наши гальваники утверждают, что прежде всего, нужны:
- Источник постоянного тока.Выбирается в зависимости от размера изделия.
- Аноды. Анодные пластины выполняют несколько функций. В первую очередь, они подводят в электролит ток, во-вторых, они возмещают убыль металла, уходящего на покрытие изделия.
- Рабочий электролит. Кислотный, щелочной или пирофосфорный раствор. Состав электролита выбирается в зависимости от исходного металла. Необходимо помнить, что любой электролит не универсален и подойдет не для всех работ.
Подготовка материала
Как правильно подготовить простой электролит меднения
Стоит отметить, что гальваника в домашних условиях медью сложна, потому что химические реактивы найти непросто. Компании, реализующие подобные продукты, не продают их без специальных документов. Но вы можете сделать все сами.
Электролит в домашних условиях возможно приготовить только при условии точного соблюдения рецептуры. В состав простейшего электролита входит:
- Дистиллированная вода (или бидистиллят).
- Медный купорос.
- Соляная или другая кислота.
Готовый раствор имеет яркий синий цвет, запаха нет. Допускается наличие некоторого осадка. Важно соблюдать все меры безопасности с химическими реактивами, особенно в домашних условиях: защита рук и глаз в первую очередь. Одежду, на которую случайно мог пролиться раствор, – лучше перевести в разряд дачной.
Хранить такую жидкость лучше в стеклянных бутылках или пластиковых канистрах, а также обязательно указать дату розлива и название раствора. Правильное хранение компонентов избавит вас от возможных проблем. Приготовление электролита должно проходить в чистой пластмассовой или стеклянной посуде.
Подготовка материала для меднения в домашних условиях

Химическое меднение — это альтернатива электрохимическому способу, но не всегда может его заменить. В этом процессе важно тщательно подготовить деталь, бесследно устранив царапины, загрязнения, сколы и т.д. Для того, чтобы обезжирить вещь, можно пускать в ход и чистые растворители, и обезжиривающие растворы.
При этом универсального метода нет – разные виды металла подвергаются очистке по-разному:
- Сталь. Обезжиривать сталь можно раствором, содержащим едкий натрий и едкий калий при 70-90 градусов по Цельсию. Это займет около 20-30 минут. Будьте аккуратны, пользуйтесь вытяжкой.
- Медь и сплавы. Обезжиривание осуществляется едким натрием, нагретым предварительно до 40°, около 10 минут.
- Чугун. Для процесса обезжиривания нужен раствор, содержащий едкий натрий, жидкое стекло, карбонат натрия и фосфат натрия при нагревании до 90°.
- Вольфрам. Меднение вольфрама в домашних условиях начинается с чистки предмета от грязи и прочих дефектов наждачной бумагой.
Техника безопасности при меднении в домашних условиях
Несмотря на возможность гальваники в домашних условиях (меднения), процесс остается опасным. В любом гальваническом процессе задействованы токсичные вещества, способные сильно нагреваться. Поэтому нужно неукоснительно соблюдать меры предосторожности.
Первое правило гальваники медью в домашних условиях – работайте только в нежилом, хорошо проветриваемом помещении. Подойдут такие места, как мастерская или гараж. Второе правило – применяемое оборудование нужно заземлить. Третье – это соблюдение личной безопасности.
Для обеспечения собственной защиты при меднении в домашних условиях нужно:
- Постоянно быть в респираторе, чтобы обезопасить дыхательные пути. лучше всего использовать вытяжку.
- Защитить руки прочными прорезиненными перчатками.
- Надеть специальную форму или клеенчатый фартук, противоожоговую обувь.
- Не забыть очки для безопасности зрительных органов.
- Не приносить в помещение еду и питье.
Перед меднением лучше заранее озаботиться прочтением специализированной литературы по данной теме. Желательно посоветоваться со специалистами данного профиля.
Гальваника в домашних условиях: меднение
Почему в гальванике столь востребована именно медь? Она имеет высокую адгезию (иными словами – сцепление) к самым разным материалам. Это значит, что она превосходно держится на изделиях из стали, вольфрама, не отлетая и не скалываясь.
Медь – красивый яркий металл, внешне напоминает самородки розово-красного оттенка. Материал проводит не только тепло, но и электрический ток – отсюда и высокий спрос в сфере электротехники и приборостроении. Однако чистую медь найти сложно. Чаще она поставляется с различными примесями.
- Отличаются малым сопротивлением, что используется в электротехнике
- Скрывает мелкие недочеты поверхности.
- Быстро окисляется, что используют для получения эффекта «антик».
Технологий меднения существует две. Одна происходит путем погружения изделия в раствор электролиты (с подачей тока или без). Второй же способ – это метод селективного нанесения покрытия без погружения в раствор. Рассмотрим оба.
Метод погружения

В домашних условиях поверхность, подвергаемую гальванике, следует скрупулезно образом обработать. Например, наждачной бумагой и щеточкой. После обязательно обезжирьте деталь и промойте.
- Анодную пластину (можно две) помещают в емкость, которую будем называть ванной. На аноды замыкают положительную клемму.
- Между анодами на любом удобном проводнике подвешивается деталь, к ней подводят отрицательный полюс от блока питания.
- Готовый раствор вливается в ванночку – при этом уровень покрытия должен быть выше, чем расположена деталь.
- После подключения электродов к источнику тока выставляют рабочий ток. Это примерно 1 А/кв.дм. покрытия.
Продолжительность работы зависит от необходимой толщины слоя, обычно от 5 минут.
Покрытие без погружения

Данный способ меднения имеет ограничения – чаще всего он подходит для реставрации поверхности. Таким способом можно нанести только небольшую толщину металла. Нет смысла покрывать таким методом изделия, которые можно меднить в ванне.
Порядок действий при гальваническом меднении в домашних условиях:
- Готовят «тампон» для нанесения покрытия. Берут медный проводник и наматывают кусок искусственной ткани (полиэстер подойдет).
- Противоположный конец проводника подсоединяют к положительной клемме источника напряжения.
- Электролитным раствором наполняют емкость – так удобнее окунать карандаш.
- Деталь аккуратно очищают и обезжиривают, а потом помещают в пустую ванночку. Там изделие подсоединяется к отрицательной клемме.
- Тампон смачивают в растворе. Затем им проводят по поверхности изделия, закрашивая ее постепенно.
Процесс длится до полного покрытия медным слоем изделия.
Особенности гальванопластики в домашних условиях
Гальванопластика — это процесс нанесения меди на проводящую или непроводящую поверхность изделия с последующим снятием покрытия с негативной матрицы. Таким образом можно получить множество очень точных копий с одного изделия. При этом, есть условие: наращивание меди толщиной не менее 200 мкм, чтобы изделие получилось прочным.
Важно учесть, что, если поверхность изделия не имеет свойств проводника, то потребуется больше усилий – а именно, особое предварительное покрытие графитом, серебром или медью. Основным металлом для осуществления гальванопластики считается медь, но можно выращивать матрицы из серебра чистотой 9999.
Обучение гальванике
Можно сделать вывод, что меднение сегодня — это один из наиболее актуальных гальванотехнических процессов, обучиться которому может каждый. Компания «6 микрон» проводит обучение по направлению «Гальваника» для всех желающих! Вы сможете выбрать удобную для Вас программу обучения, которая лучше всего подойдет для гальваники в домашних условиях и не только. Все интересующие вопросы можно задать по телефону или по электронной почте, наши технологи проконсультируют по курсам для обучения.
Видео руководство по меднению деталей в домашних условиях:
О гальванике — без формул
![]()
Что же это такое интересное, что заставило матерую валяльщицу ))) задвинуть подальше ящик с шерстью и начать создавать совсем другую красоту? Честно говоря, я занялась гальваникой с одной лишь целью — меднить и латунить фурнитуру для своих войлочных сумок, ведь так трудно подобрать все одного цвета! Но оказалось, что с большей частью фурнитуры этот номер не проходит, но зато в гальванике столько возможностей!! Не оторваться!))
О том, что такое гальваника, полным-полно статей в интернете, также там приводятся схемы электрической цепи и химический состав растворов — во все это «сильно заумное» многие не хотят или не могут вникать, да собственно, и незачем, если не собираешься этим заняться. Мне удобно думать, что мозг устроен так же, как компьютер, и любая лишняя информация, накопленная в нем, ухудшает быстродействие, не оставляет свободного пространства для творчества. Поэтому для многих вещей достаточно общего понимания, если появится необходимость — всегда можно поднакопить информации, разобраться подробнее.
Вряд ли я расскажу о гальванике лучше, чем это сделал Владислав Киселевич , его видео «Мастер-класс Гальваника в домашних условиях», по моему мнению, лучший в ру-нете.
Но все же попробую сказать пару слов о гальванике без схем и формул, специально для моих подписчиков и коллег по «войлочному цеху», озадаченных метаморфозами в моем магазине))). Очень много вопросов и догадок, иногда весьма забавных)))
Я не «окунаю всякое в жидкую медь» — это невозможно, медь — твердая. И не крашу медной краской — вещицы получаются действительно медные, твердые и прочные. И не отливаю из меди — плавить металл — это для меня пока слишком сложно! И, да — гальванику не я придумала, и омеднять растения — тоже! )))) А суть процесса в следующем.
В посудке разводится «маринад» из большого количества воды и пары флаконов химии из хозяйственного магазина. В основе химии — медный купорос, синенькие кристаллы, знакомые дачникам — его используют как удобрение. И автомобильный электролит, который автомобилисты наливают в аккумулятор. В посудку (емкость, которую называют гальванической ванной) — с одной стороны помещается кусок настоящей меди — лист или трубка (трубки легче купить, они продаются много где и используются в кондиционерах и холодильниках). Эту пластинку называют Анод. С другой стороны в емкость помещается деталька, которая хочет стать медной. Как только она погружается в раствор, ее называют Катод. (прим.: в гальванике, в отличие от электролиза, + и — меняются местами. Впрочем я и сама путаю термины, поправьте, если опять ошиблась, главное — не перепутать провода, «+» — красный — на отдающую пластину, «-» — черный — на принимающую). Точный рецепт «маринада» ищется по запросу «состав электролита для меднения», кто заинтересуется формулами и цифрами, найдет без затруднений.
Эта деталька, которую хотим покрыть медью, обязательно должна уметь проводить ток, то есть, быть металлической, или ее покрывают специальным составом, который ток проводит. Чаще всего это лак на основе графита — того самого, что в карандашах. Лак продается в магазинах для радиолюбителей, дороговат, но вполне доступен. Затем к листу меди и к детальке прикрепляются проводки и на них подается электричество — совсем небольшое, не более чем при зарядке телефона. И тут начинается волшебство. Медь с пластины «растворяется» в «маринаде» и нарастает на детальке. То есть лист меди отдает свои частички, а деталька эти частички принимает. Химический раствор и электричество помогают микро-частицам металла поменять место жительства  .
.
У меня эта конструкция выглядит так:
![]()
Чем дольше деталька находится в растворе, тем больше меди на ней нарастает, и тем тверже она становится. Процесс это довольно долгий, несколько часов, а то и дней — чем больше деталька и чем толще нужно получить слой меди — тем дольше. И тем сильнее «худеет» лист меди, отдающий себя во благо)))
Гальванику используют не только для меднения, но и для покрытия предметов другими металлами, в том числе и драгоценными. Но это в домашних условиях делать сложно и опасно — химия используется совсем другая, не из супермаркета, и отдающий металл, разумеется, должен быть тот же, которым изделие покрывается. Металлом можно покрыть любой объект или часть объекта, или сделать металлическую копию — в этом и есть смысл гальваники.
Органические предметы (растения, перышки, ракушки и т.п.) предварительно нужно полностью покрыть графитом, а потом меднить. При этом растение получается в меди, как в саркофаге — без доступа воздуха оно не гниет и не портится. Слой меди нужно делать довольно толстым — чтобы было прочно. Металлические предметы (правда, не все металлы подходят) меднятся сами, без графита.
Многие материалы нельзя погружать в элктролит, например, первое, что я сделала, конечно же — частично обмазала графитом войлочный шарик и сунула его в раствор! Если у вас есть машина и электролит хоть раз попадал на вашу одежду, вы поймете что произошло))) таки да, шерсть в раствор — нельзя! и еще много чего нельзя, без риска испортить волшебный бульончик.
Так что если надумаете вникать в тему и попробовать это увлекательное занятие — не размахивайтесь сразу на аквариум в 20 литров, попробуйте в малых количествах.
Гальваническое покрытие металлом можно нанести и на маленькую бусинку, и на целый большой памятник! Но для этого, конечно, нужна не маленькая посудка, а целый большой бассейн раствора и много-много металла. Еще — большие и криволинейные объекты покрывают металлом гальванической кистью, но это уже другая история. Так реставрируют памятники, например, гальваникой — бронзой — покрыта четверка лошадей на фронтоне Большого театра.
![]()
В домашних условиях и «для девочек» интереснее всего меднить различные природные объекты и делать из них потом украшения.
![]()
![]()
![]()
![]()
Меднение растений процесс увлекательный, но больше меня привлекло в гальванике другое — создание текстур.
Восстановление деталей электролитическим наращиванием
Нанесение электролитических (гальванических) покрытий основано на электролизе металлов. При прохождении электрического тока через электролит (раствор солей, кислот и щелочей) в нем образуются положительно заряженные ионы электролита (катионы) и отрицательно заряженные (анионы). Катионы металлов и водорода движутся к катоду и образуют на нем металлический осадок (отложение) или выделяются в виде газа. Металлический осадок называется электролитическим (гальваническим) покрытием. Анионы движутся к аноду и растворяют его, если анод растворим.
Количество осажденного вещества на катоде, согласно закону Фарадея, можно определить по формуле:
G=cIt,
где G — теоретически возможное количество осажденного металла, г; с — электрохимический эквивалент, г/А*ч; I — сила тока, A; t — продолжительность электролиза, ч.
В связи с тем, что на катоде, кроме металла, выделяется водород и протекают другие процессы, количество фактически осажденного металла меньше теоретически возможного. Отношение количества фактически осажденного металла к теоретически возможному называют выходом металла по току или к.п.д. процесса (ванны).
Толщину осажденного слоя металла определяют по формуле:
b = с*Dk*tn/100y
где Dk — плотность тока, А/дм2; n — выход металла по току; у — плотность осажденного металла, г/см3.
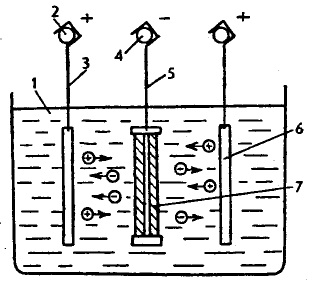
Рис. Схема электролитического осаждения металла: 1 — ванна; 2 — анодная штанга; 3 — подвеска для анодных пластин; 4 — катодная штанга; 5 — подвеска для детали; 6 — анод; 7 — деталь (катод).
При заданной толщине слоя металла по формуле можно определить продолжительность процесса.
Восстановление деталей электролитическими покрытиями имеет ряд преимуществ перед наплавкой: простота оборудования; в металле детали не происходят структурные изменения; возможность одновременно восстанавливать несколько деталей. Процесс позволяет восстанавливать детали с малыми износами и получать износостойкие покрытия. Недостаток процесса — большая трудоемкость, что ограничивает его применение при восстановлении деталей с большими износами.
Наиболее широко применяют хромирование и железнение, реже — никелирование, меднение и цинкование.
Хромирование
Электролитические покрытия хромом обладают высокой твердостью и износостойкостью. Поэтому хромированием восстанавливают износостойкие поверхности с небольшими износами (плунжерные пары, золотники распределителей, поршневые пальцы и др.).
Аноды изготовляют из свинца или сплава свинца и сурьмы. Отношение площади анодов к площади катодов принимают от 1:1 до 2:1. В процессе хромирования аноды не растворяются. Хромируемую деталь подвешивают к катоду. В качестве электролита используют раствор хромового ангидрида в воде с добавлением серной кислоты. Наибольший выход по току при соотношении хромового ангидрида и серной кислоты 100:1. Концентрация хромового ангидрида в электролитах — от 150 до 350 г/л. Плотность тока — от 15 до 80 А/дм2, напряжение — 12-15 В, температура электролита — 40—65°С.
Хромирование выполняют в ваннах, облицованных свинцом, винипластом или другим кислотостойким материалом. Стенки ванны делают двойными. Пространство между ними заполняют водой или маслом, которые являются теплоносителем для подо-грева электролита в ванне. Конструкция ванны должна предусматривать вытяжку для удаления продуктов испарения и газов, выделяющихся при электролизе. В качестве источников питания постоянного тока применяются выпрямители ВАКГ-12/6-300, ВАКГ-12/600М с напряжением 12 В, низковольтные генераторы АНД 500/250 и др. Для интенсификации процесса электролиза применяют реверсивный постоянный ток (полярность меняется по определенной программе).
Качество гальванического покрытия во многом зависит от подготовки поверхности и режима процесса. Подготовка деталей «гальваническому покрытию включает: очистку деталей; механическую обработку дяя придания правильной формы поверхностям; предварительное обезжиривание растворителями; изоляцию мест, не подлежащих покрытию, перхлорвиниловой лентой, эмалью ПХВ-715 и др. После этого деталь монтируют на подвески и проводят обезжиривание мест восстановления. Обезжиривание может проводиться химическим, электрохимическим и ультразвуковым способами.
Химическое обезжиривание проводят путем погружения деталей в горячий (60 «С) щелочной раствор и выдержки в нем от 5 до 60 мин.
Электрохимическое обезжиривание заключается в погружении деталей в щелочной раствор, через который пропускают ток. Детали служат катодом, а пластины из малоуглеродистой стали — анодом. Обезжиривание проводят при плотности тока 5-15 А/дм2, температуре электролита 60-70 «С в течение 2-3 мин на катоде и 1-2 мин на аноде. После обезжиривания промывают в воде. Чтобы получить прочное сцепление покрытий с основным металлом, необходимо провести активацию наращиваемых поверхностей (удалить пленку оксидов). Растворение оксидов проводят химическим или электрохимическим травлением. Черные металлы травят в водном растворе серной или соляной кислот. Электрохимическое травление поверхностей проводят в ванне при пропускании тока через деталь и раствор. Наиболее распространено анодное травление в ванне для электролиза (детали устанавливают на анодные штанги).
Для получения качественных хромовых покрытий необходимо соблюдать соотношение между плотностью тока и температурой электролита. Изменяя температуру электролита и плотность тока (без изменения состава электролита), можно получить три вида осадков хрома: блестящий (твердость — до НВ 900, высокая износостойкость и хрупкость), молочный (твердость — НВ 500-600, достаточная износостойкость и пластичность), матовый (наиболее твердый и хрупкий). Повышенная хрупкость матового осадка снижает его износостойкость, поэтому этот вид осадка при восстановлении деталей не используется. Блестящие осадки используют в декоративных целях.
Среднее значение выхода по току при хромировании составляет 13-15%, а скорость осаждения хрома — 0,03-0,06 мм/ч.
По причине плохой смачиваемости поверхности хромового покрытия снижается износостойкость деталей. Поэтому при восстановлении деталей, работающих в условиях повышенного удельного давления, высокой температуры и недостатка смазки (поршневые кольца, гильзы цилиндров и др.), применяют пористое хромирование. Пористость поверхности получают механическим, химическим или электрохимическим способами.
При химическом способе пористость на покрытии получают травлением в соляной или серной кислоте. При механическом способе на поверхности детали до хромирования наносят углубления резцом, накаткой или пескоструйной обработкой. В процессе хромирования подготовленный рельеф поверхности сохраняется. При электрохимическом способе детали подвергают анодной обработке в течение 8-12 мин в электролите того же состава, как и при хромировании.
Железнение
Железнением восстанавливают стальные и чугунные детали (посадочные места под подшипники, отверстия в головках шатуна и др.) с износом, достигающим 1 мм и более. При восстановлении деталей железнение применяют более широко, чем хромирование. В отличие от хромирования при железнении применяют растворимые аноды из малоуглеродистой стали. Их площадь должна быть в два раза больше покрываемой поверхности (катода). Выход по току при железнении — 85-95%, скорость осаждения металла — 0,2-0,5 мм/ч, твердость осадка НВ 700. Себестоимость восстановления деталей железнением составляет 30-50% от стоимости новых деталей.
Электролиты, применяемые при железнении, делят на три группы: хлористые, сернокислые и смешанные (сульфатно-хлористые). Наиболее распространены хлористые электролиты, которые дают лучшее качество покрытий. По температурному режиму электролиты делятся на горячие (60-90 °С) и холодные (18-20 °С). Горячие электролиты неудобны в эксплуатации, так как требуют дополнительных расходов на подогрев и контроль температуры, но они дают лучшее покрытие.
Из горячих электролитов применяют электролит, состоящий из 200—500 г/л хлористого железа, 100 г/л хлористого натрия, кислотность (рН) — 08—1,2. Режим железнения: плотность тока — 10-50 А/дм2, температура 70-80 °С.
Из холодных электролитов чаще применяют электролит, состоящий из 400-600 г/л хлористого железа, 0,5-2,0 г/л аскорбиновой кислоты, кислотность (рН) — 0,5-1,3. Режим железнения: плотность тока — 10-40 А/дм2, температура — 20-50 °С.
Подготовка поверхности детали к железнению в основном такая же, как и для хромирования. Ванны для железнения аналогичны ваннам, применяемым при хромировании. При железнении в горячем электролите внутреннюю поверхность ванны облицовывают кислотоупорным материалом (эбонитом, винипластом и т. п.).
Электролитическое осаждение железа можно вести и вневанным способом. Он позволяет восстанавливать отдельные изношенные отверстия в крупногабаритных деталях (блоки цилиндров, корпуса коробок передач задних мостов и т. д.). Кроме того, вневанное железнение позволяет повысить производительность процесса за счет циркуляции электролита и увеличения плотности тока до 300 А/дм2.
Различают три способа вневанного осаждения железа:
- струйное
- проточное
- электроконтактное
При проточном железнении изношенные отверстия превращают в местную ванночку, через которую циркулирует электролит.
Электроконтактное железнение часто называют электронатиранием, так как электроосаждение металла происходит при прохождении постоянного тока в зоне контакта детали с анодом (тампоном из фетра, войлока, непрерывно смачиваемым электролитом).
Местное железнение — частный случай проточного железнения, сущность которого в том, что восстанавливаемое отверстие герметизируют снизу, заливают электролит, устанавливают анод 3 и подключают к источнику тока.
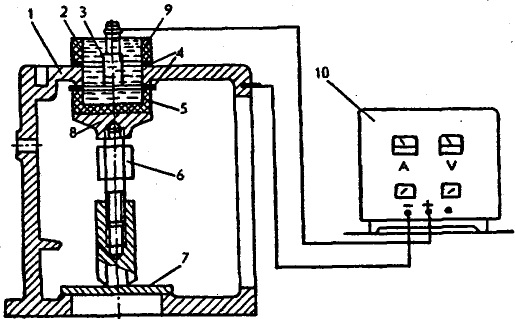
Рис. Схема местного железнения: 1 — деталь; 2 — электролит; 3 — анод; 4 — резиновые прокладки; 5- стакан; 6 — распорка; 7 — опорная плита; 8 — подставка; 9 — кольцо; 10 — выпрямитель.
