Как сделать серную кислоту в домашних условиях?
Получение кислоты в домашних условиях
Получение кислоты в домашних условиях
Попробуем получить щёлочь или кислоту в домашних условиях с помощью подручных средств. Конечно, полученный нами препарат не будет концентрированным (это достигается с помощью специального оборудования), но характерные свойства кислоты обязательно будут заметны.
Наиболее простой способ получение кислоты в домашних условиях будет основан на электролизе какого-либо раствора, который диссоциирует с образованием сульфат-иона. Иным способом получить кислоту тоже можно, но это связано или с получением сернистого ангидрида, или других химических препаратов, которых может не оказаться, да и все они достаточно опасны, чтобы с ними работать дома. Поэтому, получим, например, серную кислоту (разбавленную) из медного купороса. Та концентрация, которая получается из купороса — особо не опасна, к тому же, средств для её получения нужно немного. Итак, для опыта нам необходим источник тока (отлично подойдёт блок питания от 15 до 30 вольт). Анод (электрод подключаемый к плюсу) будем брать графитовый, — чтобы не растворялся. Катод – лучше взять виде графитовой пластинки, но можно также использовать медную фольгу.
Разведите раствор купороса опустите в него электроды. На катоде будем наблюдать выделение бурого рыхлого вещества – это медь.
Что такое медный купорос? Это медь, растворённая в серной кислоте. Приготовьтесь периодически вынимать катод » — » и очищать его от выделившейся на нём меди. Чем дольше продолжается опыт, тем раствор нашего электролита становится всё более светлым – из него удаляется медь. Если опустить наш индикатор в посветлевший раствор, то окраска изменится на алый цвет. Как-никак серная кислота! Конечно, она сильно разбавленная, но всё же проявляет свои свойства. Для того, чтобы более удостовериться в полученной кислоте возьмите пищевую соду и капните на неё полученной кислотой, — при этом должно наблюдаться бурное выделение газа – это углекислый газ. Серная кислота вступает в реакцию с пищевой содой, образуя при этом соль натрия (Na2SO4), воду и пузырьки углекислого газа.
Задуманное получилось! Для некоторых веществ она слабовата (т.к. сильно разбавлена) и реакции с ними Вы наблюдать не будете.
Конечно, можно увеличить концентрацию кислоты, если растворить в воде больше медного купороса или выпариванием излишка воды в полученной кислоте. Последнее проделывать не рекомендую, т.к. пары кислоты очень опасны.
- HCl — pH=1,0
- CCl3COOH — pH=1,2
- H2C2O2 — pH=1,3
- NaHSO4 — pH=1,4
- Винная кислота — pH=2,0
- Лимонная кислота — pH=2,1
- Молочная кислота — pH=2,4
- Салициловая кислота — pH=2,4
- Янтарная кислота — pH=2,7
- C6H5COOH — pH=2,8
- CH3COOH — pH=2,9
- NH4H2PO4 — pH=4,0
- H2S — pH=4,1
- NaH2PO4 — pH=4,5
- KH2PO4 — pH=4,7
- HCN — pH=5,1
- NH4Cl — pH=5,1
- H3BO3 — pH=5,3
- (NH4)2SO4 — pH=5,5
- Фенол — pH=5,5
- CaCO3 — pH=7,3
- (NH4)2HPO4 — pH=7,9
- C6H5COONa — pH=8,0
- NaHCO3 — pH=8,3
- CH3COONa — pH=8,9
- Na2HPO4 — pH=9,2
- Mg(OH)2 — pH=10,0
- KCN — pH=11,1
- NH3 — pH=11,3
- Na2CO3 — pH=11,6
- Na3PO4 — pH=12,0
- Ca(OH)2 — pH=12,4
- Na2SiO3 — pH=12,6
- K2S — pH=12,8
- NaOH — pH=13,0
Какая кислота кислее?!
Наверное, Вы когда-нибудь задавали вопрос «какая же из кислот более кислая ?!» «или какая из щелочей более едкая ?!» На этот вопрос можно ответить, рассмотрев значения pH растворов кислот и щелочей. Кислот очень много, поэтому рассмотрим лишь самые основные.
Значение рН раствора зависит от концентрации. Поэтому в таблице приведены значения рН водных растворов при концентрации 0,1 моль/л. Для малорастворимых соединений, отмеченных звёздочкой, указаны рН насыщенных растворов. Чем меньше значение pH раствора, тем кислота «кислее» и наоборот, чем больше значение pH раствора, тем более едкая щелочь! Получается, что, если выпить концентрированный лимонный сок, кислотность желудочного сока. понизится !? Действительно, раствор лимонной кислоты лишь разбавит более сильную соляную кислоту, содержащуюся в желудочном соке.
Кислотность воды
Большинство живых организмов могут существовать лишь в средах, близких к нейтральным. Это связано с тем, что под действием ионов Н + и ОН — многие белки, содержащие кислотные или основные группы, изменяют свою конфигурацию и заряд. А в сильнокислой и сильнощелочной средах рвётся пептидная связь, которая соединяет отдельные аминокислотные остатки в длинные белковые цепи. Из-за этого ультраосновные (сильнощелочные) растворы вызывают щелочные ожоги кожи и разрушают шёлк и шерсть, состоящие из белка. Все живые организмы вынуждены поддерживать во внутриклеточных жидкостях определённое значение кислотности среды (а так, как клетка состоит из воды на 80%, то — кислотность воды). Природная вода способна сохранять значение рН более или менее постоянным, даже если в неё извне попадает определённое количество кислоты или основания. Если в литр дистиллированной воды внести каплю концентрированной соляной кислоты, то рН понизится с 7 до 4. А если каплю соляной кислоты добавить в литр речной воды с рН=7, показатель почти не изменится. Кислоты и основания, попадающие в природную воду, нейтрализуются растворёнными в ней углекислым газом и гидрокарбонат-ионами:
Н + +НСО -3 → Н2О+СО2;
ОН — +СО2→ HCO -3 .
Можно ли сделать серную кислоту в домашних условиях
Изготовление концентрированной серной кислоты. В домашних условиях
Как вы знаете, я увлекся добычей золота и других драгметаллов из разной электроники. А для этого помимо самих золотосодержащих компонентов потребуются некоторые химические реактивы. На начальном этапе я решил не тратиться на их покупку, а постараюсь их синтезировать самостоятельно.
Причем хотелось бы обойтись без специальных химреактивов и химической посуды, чтобы все, что я делаю мог повторить любой человек. Ранее я уже писал, как я изготовил свой первый реактив, это был железный купорос:
А сегодня я расскажу, как можно в домашних условиях приготовить концентрированную серную кислоту, которая понадобиться мне для изготовления других двух кислот, соляной и азотной. А из этих двух кислот, как вы знаете готовиться царская водка.
Пятилитровая банка аккумуляторного электролита
Для нашего опыта нам потребуется аккумуляторной электролит, который продается в любом автомобильном магазине. Я купил сразу банку на 5 литров с плотностью 1,28 г/см3 (что соответствует примерно концентрации 36% ). Как наверное все знают, электролит представляет собой разбавленную серную кислоту.
И для того, чтобы получить более концентрированную кислоту, нам нужно постараться выпарить из нее всю воду. А зная ее начальную концентрацию в 36%, понятно, что нужно упарить электролит примерно в 3 раза.
Далее, нам потребуется стеклянная банка для выпаривания воды из электролита. Я взял пустую баночку из под растворимого кофе. Затем, необходимо нанести разметку на эту баночку используя какой-нибудь мерный стаканчик.
Я наклеил белые стикеры на банку и сделал отметки, указывающие на объем жидкости
Я наклеил белые стикеры на банку и сделал отметки, указывающие на объем жидкости
Так как нам нужно будет упарить раствор примерно в три раза, я нанес 3 отметки с шагом в 200 мл (см3). Далее я налил 600 мл (см3) нашего электролита.
Набрал в баночку 600 мл электролита
Набрал в баночку 600 мл электролита
Подготовил электроплитку. Вынес ее на балкон, чтобы не заниматься химией в квартире. Поставил на плитку ненужную кастрюлю, на тот случай если банка от нагрева лопнет, так банка сделана из обычного стекла и не предназначена для сильного нагревания, в отличии от специальной химической посуды.
Внутрь кастрюли насыпал небольшой слой обычного речного песка для того, чтобы нагрев происходил как можно медленнее и равномернее.
Поместил внутрь кастрюли свою баночку с электролитом и включил плитку на максимум.
Само выпаривание длиться достаточно долго. Я точно не засекал, но это порядка 4-6 часов. И после того, как наша кислота выпарилась примерно до 200 мл (см3), выключаем плитку и даем нашей баночке остыть. После чего, можно перелить нашу концентрированную серную кислоту в подходящую стеклянную бутылочку.
Переливаю концентрированную серную кислоту в бутылочку
Чтобы проверить какая же реально концентрация серной кислоты получилась в нашем опыте, я взял кухонные весы и взвесил 100 мл (см3) нашей кислоты, отмеряя ее объем 60 кубовым шприцем. У меня получилось, что 100 мл (см3) жидкости весит 167 гр. Это означает, что плотность нашей кислоты составила 1,67 гр/см3, что соответствует примерно 76% концентрации, что довольно не плохо.
Вычисляем плотность получившегося раствора
Выпарить кислоту большей концентрации было бы гораздо сложнее, т.к. чем концентрированней кислота, тем сложнее она отдает воду. Но для наших дальнейших опытов такая кислота вполне подходит, поэтому закроем нашу бутылочку и уберем ее на хранение.
Бутылочка с нашей концентрированной кислотой
Бутылочка для хранения нашей концентрированной кислоты
Бутылочка для хранения нашей концентрированной кислоты
А на этом пока все. Всем спасибо за внимание. Кому понравилось, не ленитесь, поставьте лайк. И подпишитесь на мой канал, если по какой-то причине вы еще не подписаны. Дальше я буду изготавливать соляную и азотную кислоты. Приготовлю царскую водку и растворять в ней золото. Я думаю все это будет крайне интересно. До встречи в следующей статье.
А вот небольшой видеоролик, о том как происходил весь процесс подготовки и выпаривания кислоты.
Ответы Mail.ru: как в домашних условиях сделать серную кислоту. для домашних хим. эксперементов.
Максим Ю. Волков
Изготавливается из электролита для свинцовых аккумуляторов (приобретается в магазине на авторынке) . Это 36% раствор кислоты в воде. Небольшое количество электролита выливается в какую-нибудь широкую стеклянную ёмкость вроде маленькой банки (отрезанное дно от бутылки с высотой стенок около 4 см также подойдёт) . Для безопасности лучше работать с малыми порциями электролита (по 10-20 мл) . Так вот, эта банка с электролитом ставится на песочную баню. Баня . это песок слоем 5-10 см насыпан например в литровую эмалированную кружку (кастрюлю, что угодно, главное из металла) . Вся эта конструкция ставится на слабый огонь газовой плиты. Песок прогревается и прогревает электролит. При нагревании разбавленная H2SO4 теряет воду, пока концентрация кислоты не достигнет примерно 98%. Продолжайте нагревать, пока жидкость не начнёт дымить. Как только появился слабый дымок . выключайте газ. Не перегрейте кислоту, иначе вся кухня заполнится едкими и без сомнения очень вредными парами серной кислоты. Продержите жидкость в остывающей бане минут 5-10. Если начал идти сильный едкий дым . сразу вынимайте банку с кислотой из песка и переносите её на какую-нибудь деревянную подставку . Закройте банку металлической или стеклянной крышкой. Конц. серная кислота впитывает влагу из воздуха, поэтому как можно быстрее перелейте её в ёмкость для хранения и хорошенько закройте. Во время процедуры на случай того, если вы опрокинете ёмкость с кислотой или если стекло банки треснет и та выльется на раскалённый песок держите поблизости бутылку с раствором соды и носите очки (хотя бы какие-нибудь солнцезащитные) . Обращайтесь с раствором также осторожно, как с нитроглицерином . концентрированная серная кислота, да ещё нагретая градусов до 200-300, проест в ваших руках дыру ещё до того, как вы это успеете заметить.
её можно купить там же, где продаются автомобильные аккумуляторы
накрайняк купить их самих
почитай в интернете, как из них её вырабатывают
кислоту высокой концентрации из неё получают также кипячением
в интернет
Купите электролит для аккумуляторов — это раствор серной кислоты, не помню какой концентрации, плотностью примерно 1,27 или около того. Подходит для всех домашних экспериментов, где не требуется высокая концентрация.
Изготавливается из электролита для свинцовых аккумуляторов (приобретается в магазине на авторынке) . Это 36% раствор кислоты в воде. Небольшое количество электролита выливается в какую-нибудь широкую стеклянную ёмкость вроде маленькой банки (отрезанное дно от бутылки с высотой стенок около 4 см также подойдёт) . Для безопасности лучше работать с малыми порциями электролита (по 10-20 мл) . Так вот, эта банка с электролитом ставится на песочную баню. Баня . это песок слоем 5-10 см насыпан например в литровую эмалированную кружку (кастрюлю, что угодно, главное из металла) . Вся эта конструкция ставится на слабый огонь газовой плиты. Песок прогревается и прогревает электролит. При нагревании разбавленная H2SO4 теряет воду, пока концентрация кислоты не достигнет примерно 98%. Продолжайте нагревать, пока жидкость не начнёт дымить. Как только появился слабый дымок . выключайте газ. Не перегрейте кислоту, иначе вся кухня заполнится едкими и без сомнения очень вредными парами серной кислоты. Продержите жидкость в остывающей бане минут 5-10. Если начал идти сильный едкий дым . сразу вынимайте банку с кислотой из песка и переносите её на какую-нибудь деревянную подставку . Закройте банку металлической или стеклянной крышкой. Конц. серная кислота впитывает влагу из воздуха, поэтому как можно быстрее перелейте её в ёмкость для хранения и хорошенько закройте. Во время процедуры на случай того, если вы опрокинете ёмкость с кислотой или если стекло банки треснет и та выльется на раскалённый песок держите поблизости бутылку с раствором соды и носите очки (хотя бы какие-нибудь солнцезащитные) . Обращайтесь с раствором также осторожно, как с нитроглицерином . концентрированная серная кислота, да ещё нагретая градусов до 200-300, проест в ваших руках дыру ещё до того, как вы это успеете заметить. Купите электролит для аккумуляторов — это раствор серной кислоты, не помню какой концентрации, плотностью примерно 1,27 или около того. Подходит для всех домашних экспериментов, где не требуется высокая концентрация.
Готовим электролит для аккумуляторов в домашних условиях самостоятельно
В настоящее время выбор аккумуляторных батарей огромен — в продаже можно найти уже готовые к использованию источники питания, а также сухозаряженные батареи, которые требуют осуществить приготовление электролита и его заливку до начала эксплуатации. Дальнейшее обслуживание аккумуляторов многие часто осуществляют в сервисах. По разным причинам может возникнуть необходимость самостоятельно приготовить раствор. Чтобы это мероприятие увенчалось успехом, следует знать, как сделать электролит в домашних условиях.
Что такое электролит?

Электролит — электропроводящий раствор, содержащий в своём составе дистиллированную воду и серную кислоту, едкий калий или натрий в зависимости от типа источника питания.
Концентрация серной кислоты в АКБ
Этот показатель кислотности напрямую зависит от необходимой плотности электролита. Изначально средняя концентрация этого раствора в автомобильном аккумуляторе — около 40% в зависимости от температуры и климата, в которых используется источник питания. Во время эксплуатации концентрация кислоты падает до 10–20%, что сказывается на работоспособности АКБ.
Вместе с тем стоит понимать, что аккумуляторная серная составляющая — наичистейшая жидкость, которая на 93% состоит непосредственно из кислоты остальные 7% — примеси. На территории России производство этого химиката строго регламентировано — продукция должна соответствовать требованиям ГОСТ.
Отличия электролитов для разных типов аккумуляторов
Несмотря на то что принцип работы раствора одинаков для разных источников питания, следует знать о некоторых различиях составов. В зависимости от состава принято выделять щелочной и кислотный электролиты.
Щелочные АКБ

Этот вид источников питания характеризуется наличием гидроокиси никеля, окиси бария и графита. Электролит в этом виде аккумуляторов представляет собой 20% раствор едкого калия. Традиционно используется добавка моногидрата лития, которая позволяет продлить срок эксплуатации АКБ.
Щелочные источники питания отличаются отсутствием взаимодействия калийного раствора с веществами, образуемыми во время работы аккумулятора, что способствует аксимальному уменьшению расхода.
Кислотные АКБ

Этот вид источников питания является одним из самых традиционных, поэтому и раствор в них знаком многим — смесь дистиллированной воды и серного раствора. Концентрат электролита для свинцово-кислотных аккумуляторов дешёво стоит и характеризуется способностью проводить ток большой величины. Плотность жидкости должна соответствовать климатическим показателям.
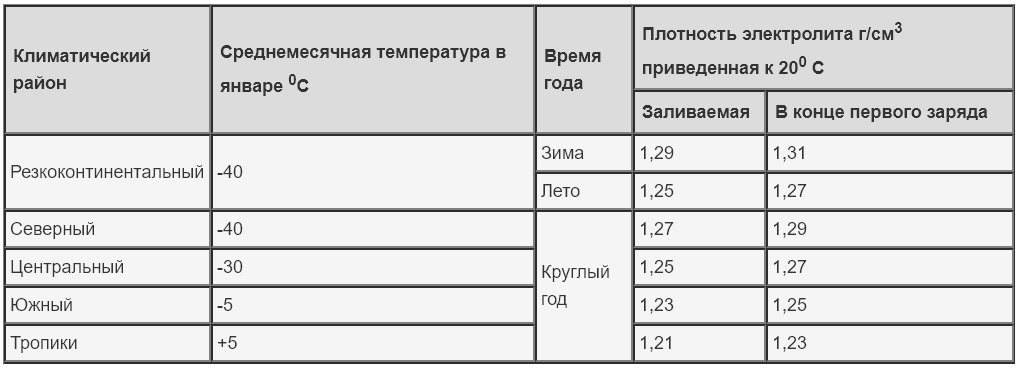
Таблица 1. Рекомендуемая плотность электролита
Другие виды АКБ: можно ли приготовить электролит для них самостоятельно?

Отдельно хотелось бы обратить внимание на современные свинцово-кислотные источники питания — гелевые и AGM. Они также могут быть заправлены собственноручно приготовленным раствором, который в них находится в специфической форме — в виде геля или внутри сепараторов. Для заправки гелевых аккумуляторов понадобится ещё один химический компонент — силикагель, который загустит кислотный раствор.
Кадмиевоникелевые и железоникелевые аккумуляторы
В отличие от свинцовых источников питания, кадмиево- и железоникелевые заливаются щелочным растовром, который является смесью дистиллированной воды и едкого калия или натрия. Гидроксид лития, входящий в состав этого раствора для определённых температурных режимов, позволяет увеличить срок службы АКБ.

Таблица 2. Состав и плотность электролита для кадмиево- и железоникелевых и аккумуляторов.
Железоникелевые источники питания рекомендуется эксплуатировать в тех же условиях, что и кадмиево-никелевые. Однако стоит отметить, что они более восприимчивы к низким температурам. Поэтому их следует использовать до минус 20 градусов.
Как правильно приготовить электролит в домашних условиях: техника безопасности
Приготовление раствора — работа с кислотами и щелочами, поэтому соблюдение мер предосторожности необходимо для самых опытных людей. Перед началом действия подготовьте средства защиты:
- резиновые перчатки
- одежду и фартук, устойчивый химическим веществам;
- защитные очки;
- нашатырный спирт, кальцинированную соду или борный раствор, чтобы нейтрализовать кислоту и щёлочь.
Оборудование
Для приготовления аккумуляторного электролита помимо самого источника питания потребуются следующие предметы:
- ёмкость и палочка, устойчивые к воздействию кислот и щелочей;
- дистиллированная вода;
- инструменты для измерения уровня, плотности и температуры раствора;
- аккумуляторная серная жидкость — для кислотной АКБ, твёрдые или жидкие щелочи, литий — для соответствующих видов АКБ, силикагель — для гелевых аккумуляторов.
Последовательность процесса: делаем электролит для кислотно-свинцового источника питания
Перед началом работ ознакомьтесь с информацией, приведённой в таблице 3. Она позволит выбрать необходимый объем жидкостей. В аккумуляторах залито от 2,6 до 3,7 литра кислотного раствора. Мы рекомендуем разводить примерно 4л электролита.
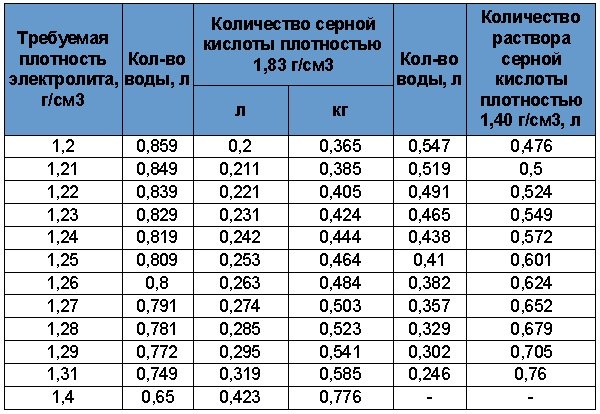
Таблица 3. Пропорции воды и серной кислоты.
- В ёмкость, устойчивую к едким веществам, налейте нужный объем воды.
- Разбавлять воду кислотой следует постепенно.
- По окончании процесса вливания замеряйте плотность получившегося электролита с помощью ареометра.
- Дайте составу отстояться около 12 часов.
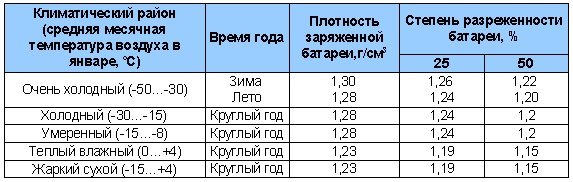
Таблица 4. Плотность электролита для разных климатов.
Концентрация кислотного раствора должна соотноситься с минимальной температурой, при которой эксплуатируется аккумулятор. Если жидкость получилась слишком концентрированной, её необходимо разбавить дистиллированной водой.
Смотрите видео, как измерить плотность электролита.
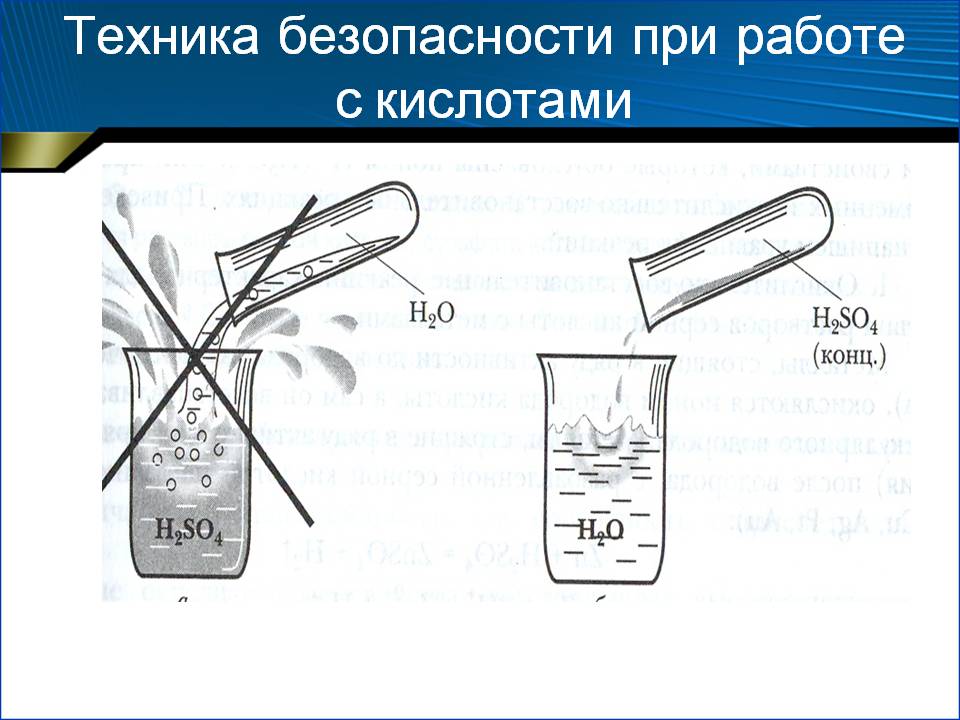
Обращаем ваше внимание, что во время смешивания компонентов выделяется тепло. В подготовленный аккумулятор следует заливать остывший раствор.
Способ развести электролит для щелочного источника питания
Плотность и количество электролита в таких аккумуляторах указана в инструкции по эксплуатации источника питания или на сайте компании-производителя.
Необходимая плотность раствора
Количество твёрдой щелочи равняется количеству электролита, разделенному на
При появлении осадка следует его перемешивать. Если к концу отстаивания он остаётся, слейте электролит так, чтобы осадок не попал в аккумулятор — это приведёт к уменьшению срока его эксплуатации.
После приведения раствора к комнатной температуре и его заливке в аккумулятор, источник питания необходимо полностью зарядить током, составляющим 10% от ёмкости АКБ (60Ач — 6А).
Как видите, приготовление раствора электролита не такое сложное дело. Главное, следует чётко определиться с необходимым количеством ингредиентов и помнить о безопасности. Вы пробовали развести электролит своими руками? Поделитесь опытом с нашими читателями в комментариях.
Как своими руками сделать паяльную кислоту, для чего она нужна и чем смыть состав после пайки
Качество паяльных работ зависит не только от сноровки домашнего мастера, но и от вспомогательных средств, которые облегчают процесс и устраняют факторы, препятствующие соединению металлических элементов между собой. Одним из таких веществ является паяльная кислота.
Давайте обсудим, какие виды паяльной кислоты чаще всего находят применение на практике, зачем и на каком этапе работ она используется, где можно купить кислотный флюс, можно ли сделать аналог паяльной кислоты самостоятельно в домашних условиях и из чего, какие меры предосторожности необходимо соблюдать при этом.

Что такое паяльная кислота и для чего она нужна?
Паяльная кислота – это химическое вещество, с помощью которого подготавливают металлические поверхности к пайке. Большинство металлов, находясь во внешней среде и контактируя с воздухом и парами воды, частично окисляется. В результате этого окисления поверхностный слой металла преобразуется в оксидную пленку. Этот слой покрывает металл и препятствует контакту припоя с его поверхностью.

Удалить оксидный слой можно двумя способами: механическим и химическим. При первом способе его сошлифовывают с помощью наждачной бумаги или шлифовального диска. Подобная обработка годится для крупных деталей простой формы. Для мелких элементов или деталей со сложной конфигурацией механический способ не подходит, поэтому приходится искать другой выход.
В этом случае металлическая поверхность обрабатывается кислотным флюсом. С ее помощью можно полностью растворить оксидную пленку, а также удалить все жировые загрязнения, которые также мешают качественной пайке. Обработка паяльной кислотой – несложная процедура, которую легко выполнить дома.
Разновидности кислоты для пайки и особенности их применения
В роли кислот для пайки могут выступать несколько соединений. Они имеют различные химические формулы и по-разному ведут себя по отношению к разным металлам или сплавам. Составы нескольких наиболее популярных видов паяльной кислоты, применяемых на практике, и их особенности:

- Хлороцинковый флюс. Его более правильное название – тетрахлорцинковая кислота, а химическая формула выглядит так: H2ZnCl4. Данное вещество получается в результате растворения цинка в соляной кислоте. Хлороцинковый флюс хорошо плавится при температуре 322°С, которая близка к температуре паяния. Он не разлагается и полностью растворяет оксидную пленку на металле. При этом хлороцинковый флюс не связывается химически с самим металлом, а также входящими в состав припоя оловом и свинцом, что очень важно для качественной пайки. Хлороцинковый флюс хорошо показал себя в работе с алюминием. Это вещество используют как в чистом виде, так и в виде припоев и флюсов промышленного изготовления. Пример готового продукта этого типа: «Rexant 09-3610» (89 руб. за 30 мл).
- Олеиновая кислота (технический олеин). Это вещество используют не в чистом виде, а как компонент в составе олеинового флюса. Он прекрасно обезжиривает металл и растворяет оксидную пленку. Чаще всего с его помощью спаивают медные или алюминиевые детали. При этом олеиновый флюс обволакивает поверхность, перекрывая доступ кислорода из воздуха и предотвращая новое окисление. Флюс этого типа невозможно изготовить в домашних условиях, для этого требуется специальная аппаратура, поэтому его покупают в готовом виде. Один из вариантов такой смеси содержит 100 г канифоли, 30 г пальмитиновой, 25 г стеариновой и 45 г олеиновой кислоты. В процессе пайки при температуре свыше 200°C выполнивший свою функцию олеин испаряется. Сфера применения: деликатная пайка радиодеталей и микросхем. 0,9 кг технической олеиновой кислоты стоят 400 руб.
- Ортофосфорная кислота (H3PO4). Удаляет слой оксида с металлов и препятствует их дальнейшему окислению. Применяется при пайке элементов из железа и содержащих его сплавов. Для получения ортофосфорного флюса в домашних условиях кислоту смешивают с другими компонентами, например, с канифолью. Пример флюса, в состав которого входит ортофосфорная кислота: «Ф-38 Н» (225 руб. за 30 мл).
- Ацетилсалициловая кислота (аспирин). Это вещество может применяться не только как лекарственный препарат. Нанесенная на подлежащую припаиванию металлическую деталь кислота растворяет окислы, но не портит сам металл. Хорошо подходит для работы с медью, золотом и серебром. Ацетилсалициловую кислоту используют как в чистом виде, так и в смеси с вазелином. Существующий готовый флюс на основе ацетилсалициловой кислоты называется «ВТС», его упаковка весом 20 г обойдется в 35 руб.
Как самостоятельно сделать паяльную кислоту?
Паяльная кислота продается в специализированных магазинах радиотехники. Ее также можно заказать через интернет. Однако возникают ситуации, когда срочно нужна кислота для пайки, но нет возможности ее купить. Решить эту проблему помогут несколько проверенных рецептов. Большинство смесей имеют несложный состав, и их можно приготовить своими руками:

- Самодельный хлороцинковый флюс. В 1000 мл концентрированной соляной кислоты растворяют 400 г гранулированного цинка. Следует помнить, что металлический цинк при взаимодействии с соляной кислотой вытесняет из нее водород, который в виде пузырьков выходит из жидкости в воздух. Содержащийся в воздухе кислород и водород образуют гремучую смесь, которая может взорваться от малейшей искры. В связи с этим следует соблюдать меры предосторожности: не курить, не использовать источники открытого огня и предотвращать возникновение искр в помещении, где ведутся работы. Нельзя работать в помещении с неисправной электропроводкой. Также следует максимально предотвратить скопление водорода в воздухе. Для этого растворять цинк лучше на улице, балконе или возле открытого окна.
- Аспириново-глицериновая смесь. В горячем глицерине растворяют измельченные в порошок таблетки аспирина. Другой способ изготовления флюса на основе ацетилсалициловой кислоты заключается в смешивании аспиринового порошка с техническим вазелином. Оптимальные пропорции для этой смеси – 1:2, то есть вазелина должно быть в два раза больше, чем ацетилсалициловой кислоты.
- С ортофосфорной кислотой. В зависимости от задач ортофосфорную кислоту наносят на место пайки в чистом виде, либо в составе смесей. Для приготовления одного из вариантов смеси к одной части ортофосфорной кислоты добавляют такое же количество хлористого цинка. В другом составе смешивают кислоту, канифоль, этиловый спирт и воду. Ортофосфорную кислоту применяют при пайке деталей из нержавеющей стали, никеля, алюминия, меди, низколегированной стали, хромоникелевых сплавов.
Меры безопасности при изготовлении и использовании средства

Для обеспечения собственной безопасности и исключения вреда для здоровья следует пользоваться такими индивидуальными средствами защиты, как перчатки, очки и респиратор. В рабочем помещении категорически запрещено курить и пользоваться источниками открытого огня. Большинство кислот разъедает металл, поэтому смешивать компоненты нужно в стеклянной или керамической посуде.
По этой же причине остатки реактивов нельзя сливать в канализацию, т. к. они могут испортить трубы. Все отходы и излишки желательно нейтрализовать и слить в почву. Для нейтрализации активных кислот, таких, как соляная и ортофосфорная, используют различные щелочные растворы, например, мыльный или кальцинированной соды.

Необходимо позаботиться о хорошей вентиляции рабочего места. В мастерской желательно оборудовать вытяжной шкаф. Если это невозможно, то соединять реактивы и паять следует на открытом воздухе или возле широко раскрытого окна или двери.
При случайном попадании составов на руки или другие части тела их обильно промывают проточной водой в течение 10 минут. В случае попадания кислотных смесей рекомендуется обработать пораженное место раствором питьевой соды.

Как смыть кислоту после пайки?
По силе воздействия кислотные флюсы можно поделить на активные и неактивные. Какие у них особенности? Примеры активных: соляноцинковый, ортофосфорный. Флюсы этого типа применяются при пайке меди, железа, никеля, углеродистых сталей или алюминия. Они хорошо удаляют окись, но, оставшись на поверхности металла, вызывают его коррозию. После окончания работ их необходимо нейтрализовать и смыть с помощью раствора кальцинированной соды или воды с мылом. В некоторых случаях рекомендуется пользоваться спиртом или ацетоном.

Нейтральные флюсы, например. олеиновый, применяют для пайки радиодеталей и печатных плат. Они безопасны в плане коррозии и не требуют обязательного смывания. При необходимости остатки флюса удаляются спиртом, ацетоном или водой.
Можно ли обойтись без кислоты?
В ряде случаев спаять детали можно и без кислоты. Для удаления оксидного слоя крупные предметы обрабатывают наждачной бумагой непосредственно перед пайкой. В ходе работ рекомендуется использовать такие нейтральные флюсы, как канифоль или ЛТИ-120. Они не содержат активных кислотных компонентов, но довольно хорошо справляются с защитой поверхности от контакта с воздухом.

Как правильно хранить состав?
Оставшийся после паяльных работ избыток флюса необязательно выбрасывать. Его можно сохранить в хорошем состоянии, если придерживаться следующих правил:
- не использовать для хранения посуду из металла или с металлической крышкой;
- надежнее всего хранить кислотный флюс в герметично закрывающейся стеклянной, керамической или пластмассовой емкости;
- место хранения должно быть темным, сухим и прохладным.
Аффинаж серебра в домашних условиях с помощью электролиза, растворение в азотной кислоте, осаждение медью, необходимое оборудование
Серебро само по себе достаточно часто используется для покрытия различных элементов техники и электронного оборудования. Его повторное использование предусматривает предварительную очистку от лигатуры. Физические действия, направленные на растворение драгметалла с помощью химических веществ называется аффинажем. Существует множество методов, помогающих получить чистое техническое серебро, которые можно использовать дома и для промышленной переработки.
- Предметы, содержащие серебро годные для аффинажа
- Что такое аффинаж
- Необходимое оборудование
- Инструменты для работы
- Химические материалы и сырье
- Методы аффинажа серебра. Пошаговая инструкция
- Электролитический для технического серебра
- Аффинаж серебра азотной кислотой и осаждение медью
- Купелирование со свинцом
- Безкислотный аффинаж
- Аффинаж из фотопленки
- Суть аффинажа серебра в домашних условиях электролитом
- Меры предосторожности для домашней добыче металла
- Сколько стоит аффинированное серебро
- Куда можно реализовать трофей
- Применение технического серебра
- Видео: методы аффинажа серебра
- Рубрика вопрос — ответ
- Как растворить серебро?
- Очистка серебра от примесей в домашних условиях, как?
- Комментарий ювелира
Предметы, содержащие серебро годные для аффинажа
Много серебра, которое можно использовать для технических целей содержится в советской радиоаппаратуре, электрическом промышленном оборудовании. Также металлом покрывались контакты следующих устройств, уже вышедших из строя:
- шахтных магнитных пускателей;
- шахтных подстанций;
- реле;
- флажков (керамических конденсаторов);
- термодатчиков;
- аппаратуры связи;
- рентгеновских, фотопленках;
- электро-вычислительное оборудование разных периодов производства.
Что такое аффинаж
Аффинаж серебра направленна получение чистого благородного металла. Именно процесс отделения его от различных примесей с использованием специальных технологий называется аффинажем. Существует несколько разных способов очистки, которые применяются поэтапно, требуют определенных знаний и навыков.
 Аффинаж серебра
Аффинаж серебра
Необходимое оборудование
Разные методы предусматривают использование специального оборудования. К такому относят:
- печь;
- тигель, имеющий форму чашки;
- блок питания;
- горелку;
- ячейки из песчаника (пластика);
- посуду, предназначенную для работы с химическими веществами.
Инструменты для работы
Для процесса очистки также необходимы следующие инструменты:
- емкости из стекла;
- стеклянная палочка;
- шина (трубка) из меди;
- фланг;
- круглогубцы;
- кусачки;
- шило;
- тканевые мешочки.
Химические материалы и сырье
При очистке драгметалла также используются:
- различные кислоты;
- щелочные вещества;
- вода.
Методы аффинажа серебра. Пошаговая инструкция
Существует множество методов направленных на отделение благородного металла от примесей дома. Наиболее популярными из них являются:
- Химический способ очистки – осуществляется с применением кислот и сульфит натрия. Не относится к сложным процедурам, но требует соблюдения некоторых правил.По итогу не всегда удается получитьдрагметалл высокого качества.
- Электролитическое отделение – применяется если нет возможности купить и использовать кислоты. Является самым эффективным методом очистки от примесей нитрата серебра.
- Безкислотный аффинаж –очистка осуществляется без применения кислот, после предварительной подготовки металла.
- Купелирование – применяется для низкопробного драгметалла. Метод требует использования специального оборудования. Способствует быстрому очищению низкопробного металл.
- Получение серебра из фотопленки – применяется для обработки фотобумаги, пленки для рентгена, флюорографии. Выделяет незначительное количество технического драгметалла.
 Аффинаж серебра методом электролиза
Аффинаж серебра методом электролиза
Электролитический для технического серебра
Аффинаж серебра электролизом заключается в использовании селитрыаммиачной и серной кислоты, разогретой до определенной температуры. Разогревание этих компонентов способствует образованию азотной кислоты, которая собственно и способна выделять технический металл.
Для проведения аффинажа нужно:
- стеклянные емкости для кислоты;
- электролит серной кислоты;
- селитра;
- песочная баня;
- стружка цинка;
- сольповаренная;
- соляная кислота;
- горячая вода.
Чтобы растворить драгметалл, используя этот метод, понадобится 1 литр водного электролита, 0,5 кг селитры из расчета на 100 грамм выделяемого металла. Растворение будет осуществляться на протяжении суток.
Формула успешного растворения серебра заключается в следующих действиях:
- Стеклянную трехлитровую емкость необходимо установить на песочной бане, подогреваемой электрической печкой.
- Емкость наполняется 150 гр. селитры, 300 мл электролита.
- При нагревании эти вещества начинают реагировать. Реакция на вид напоминает кипение, с выделением красного газа. При этом цвет жидкости меняется, становится синим.
- Когда реагирование прекращается, туда же добавляются остальные химические компоненты, пропорционально количеству выделяемого металла. В раствор погружаются элементы, покрытые драгоценным металлом.
- Когда металл полностью растворится, можно приступать к получению хлорида серебра. Для этого емкость наполняется теплой водой, почти до верха. Туда же всыпается соль, до тех пор, пока на поверхности не появятся хлопья.
- Теперь можно приступать к фильтрации хлорида. Отделив хлопья от жидкости, туда же заливают соляную кислоту. Кислота должна быть примерно на 2 см выше осадка. К раствору добавляется стружка цинка как восстановитель, который реагирует с кислотой, вытесняя серебряный металл. Процесс сопровождается выделением водорода.
- Уже через полчаса после осаждения образуется угольный осадок, который и является серебром.
- Нужно проверить есть ли в растворе кислота: для этого жидкость колотят стружкой цинка, в результате чего запускается реакция растворения. Если такой реакции нет, емкость следует наполнить соляной кислоты, это необходимо для того, чтобы очистить полученный металл от цинка, который делает его хрупким, не пригодным для дальнейшего использования.
- По окончанию реакции образовавшийся металлизированный осадок промывается. Теперь можно перейти к сплавлению хлопьев с помощью тигли и горелки.
